
- 高级人才招聘
- 中、初级专业技术人才招聘
- 管理、支撑岗位招聘
- 博士后招聘
近日,中国科学院微生物研究所李明团队与刘宏伟团队合作,在工程菌生物安全控制领域取得新进展。研究团队提出一种将毒素–抗毒素模块与CRISPR-Cas系统偶联的生物封控新策略——ATTACH(Associate Toxin–Antitoxin with CRISPR-Cas to Harness engineered microbes),构建了具有遗传稳定性的双层生物安全开关,为工程微生物的安全应用提供了新的思路。相关研究成果已发表在《核酸研究》(Nucleic Acids Research)上。
工程微生物在生物制造、疾病治疗和环境修复等领域具有广泛应用前景,但它们在环境中可能发生的扩散也引发了生物安全方面的担忧,因此亟需发展稳定、可靠的生物封控技术。目前,基于CRISPR-Cas系统构建的“自杀开关”(kill switch)虽可用于工程菌封控,但在长期培养和强选择压力下,容易因基因突变而失效,导致逃逸细胞的出现,从而制约了实际应用。
基于前期对于CRISPR护卫系统CreTA的原创发现(Science,2021),研究团队设计并构建了生物封控系统ATTACH。该系统通过“双保险”机制进行封控:首先,CRISPR-Cas系统作为主要杀伤模块,在诱导条件下通过Cas3介导的染色体大规模降解快速杀灭工程菌;其次,当CRISPR效应蛋白基因突变或蛋白失活时,毒素–抗毒素模块释放毒素并触发细胞死亡,从而清除逃逸细胞,显著提高了封控系统的稳定性和效率。
在此基础上,研究人员通过优化迭代,构建了无需抗生素筛选标记的ATTACH3,并在益生菌Nissle 1917中进行了评估。在小鼠肠道模型中,诱导ATTACH系统168小时后,工程菌的逃逸率接近10⁻9,超出美国国立卫生研究院(NIH)推荐的生物安全标准(10⁻8)约10倍。进一步应用研究表明,该系统对工程菌生长及番茄红素(抗氧化剂)的合成产量均无明显影响,并在多种细菌中展现出跨物种“即插即用”特性。该研究为益生菌及其他工程微生物的安全应用提供了重要技术支撑。
中国科学院微生物研究所助理研究员赵会伟、客座研究生周涛、博士研究生张明以及山东农业大学副教授汪城墙为该论文的共同第一作者,微生物所李明研究员、刘宏伟研究员和赵会伟助理研究员为论文的共同通讯作者。该研究得到国家重点研发计划、中国科学院战略性先导科技专项、国家自然科学基金和中国科学院青年创新促进会等项目资助。
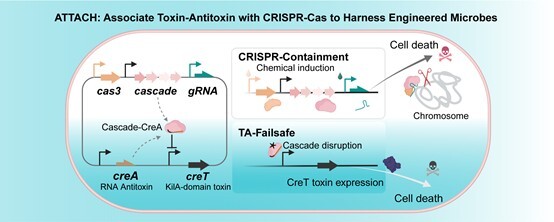
基于CRISPR偶联毒素–抗毒素系统开发的生物封控技术ATTACH
论文链接:https://doi.org/10.1093/nar/gkag213
附件下载: